免疫检查点阻断(ICB)疗法的开发和应用改变了癌症治疗格局。然而,肿瘤会采用各种策略来逃逸免疫监视,从而导致免疫治疗无响应或耐药。
中枢神经系统(CNS)具有多种抑制免疫反应的特性。肿瘤和CNS是否共享类似的免疫抑制程序尚不明确。
2024年5月31日,中山大学附属孙逸仙纪念医院苏士成、陆艺文等人在癌症领域顶级期刊 Cancer Cell 上发表了题为:Tumor cells impair immunological synapse formation via central nervous system-enriched metabolite 的研究论文。
该研究分析了HER2阳性乳腺癌患者接受抗PD-L1单抗、抗HER2单抗及化疗治疗后的肿瘤多组学数据,发现在中枢神经系统(CNS)中富集的N-乙酰转移酶8样蛋白(NAT8L)也在患者肿瘤中高表达,且与不良预后相关,在肿瘤和神经炎症中,NAT8L通过其代谢产物N-乙酰天冬氨酸(NAA)抑制细胞毒性细胞,NAA通过诱导核纤层蛋白A-K542的乙酰化来抑制免疫突触形成,从而抑制免疫效应细胞对肿瘤的杀伤作用。
这项研究发现了肿瘤细胞通过模拟中枢神经系统(CNS)的抗炎机制来逃避抗肿瘤免疫,并揭示了NAT8L是一个潜在的肿瘤免疫治疗新靶点,靶向抑制NAT8L可以增强抗癌药物的疗效。

抗肿瘤免疫反应在许多常规的肿瘤治疗方法的治疗效果中也扮演着至关重要的角色,例如单克隆抗体(mAb)。自然杀伤(NK)细胞可以裂解与抗体结合的癌细胞,也就是所谓的抗体依赖的细胞介导的细胞毒作用(简称ADCC效应)。此外,单克隆抗体还可以增强树突状细胞(DC)对肿瘤抗原的摄取和呈递,从而启动抗肿瘤T细胞反应。
之前的一些临床前研究已经表明,抗HER2单抗和抗PD-1/PD-L1单抗在促进抗肿瘤免疫方面有协同作用。这些发现已被一项3期临床试验(KEYNOTE-811试验)证实,基于该试验的结果,抗PD-1单抗(pembrolizumab)与抗HER2单抗(trastuzumab)和化疗联合治疗已被批准作为HER2阳性的晚期或转移性胃腺癌患者的一线治疗方案。然而,另一项3期临床试验(IMpassion050试验)显示,在HER2阳性乳腺癌患者中,新辅助抗PD-L1单抗联合抗HER2单抗体和化疗并不能提高患者的病理完全缓解率。
因此,迫切需要阐明乳腺癌是如何抑制由免疫检查点阻断(ICB)疗法和抗HER2单抗释放的抗肿瘤免疫反应的。
作为癌症的标志之一,异常代谢会抑制抗肿瘤免疫,从而导致对肿瘤免疫疗法的抵抗。肿瘤代谢重编程会减少免疫效应细胞的浸润,抑制抗原激活并阻止效应细胞的扩增。
由抗HER2单抗和抗PD-L1单抗介导的抗肿瘤作用依赖于效应细胞的细胞毒性,这需要直接的细胞间接触。在激活信号传递后,NK细胞和CD8+T细胞通过一种特殊的接触点——免疫突触(Immunological Synapse,IS)紧密连接,并通过免疫突触向目标细胞释放裂解性颗粒(Lytic granules)。然而,免疫突触的形成是否可以由肿瘤代谢变化介导,目前尚不清楚。
在这项最新研究中,研究团队进行了一项前瞻性、单臂、2期临床试验(KN035-TH-HER2试验),其中HER2阳性的复发或转移性乳腺癌患者接受抗PD-L1单抗、抗HER2单抗和化疗药物多西他赛的联合治疗。研究团队对敏感患者和耐药患者的肿瘤活检样本进行了无偏倚多组学分析,以探究决定乳腺癌对免疫检查点阻断(ICB)和抗HER2单抗响应的潜在机制。
分析结果显示,原本在中枢神经系统(CNS)中富集的N-乙酰转移酶8样蛋白(NAT8L)及其代谢产物N-乙酰天冬氨酸(NAA)在耐药患者的肿瘤中被过度表达。在CNS中,NAA在脑部炎症期间被释放。NAT8L通过抑制自然杀伤(NK)细胞和CD8+T细胞的细胞毒性作用来减轻脑部炎症并损害抗肿瘤免疫。NAA会通过促进PCAF对lamin A-K542的乙酰化作用来干扰免疫突触(IS)的形成,从而抑制lamin A与SUN2之间的整合,并影响裂解性颗粒(Lytic granules)的极化。
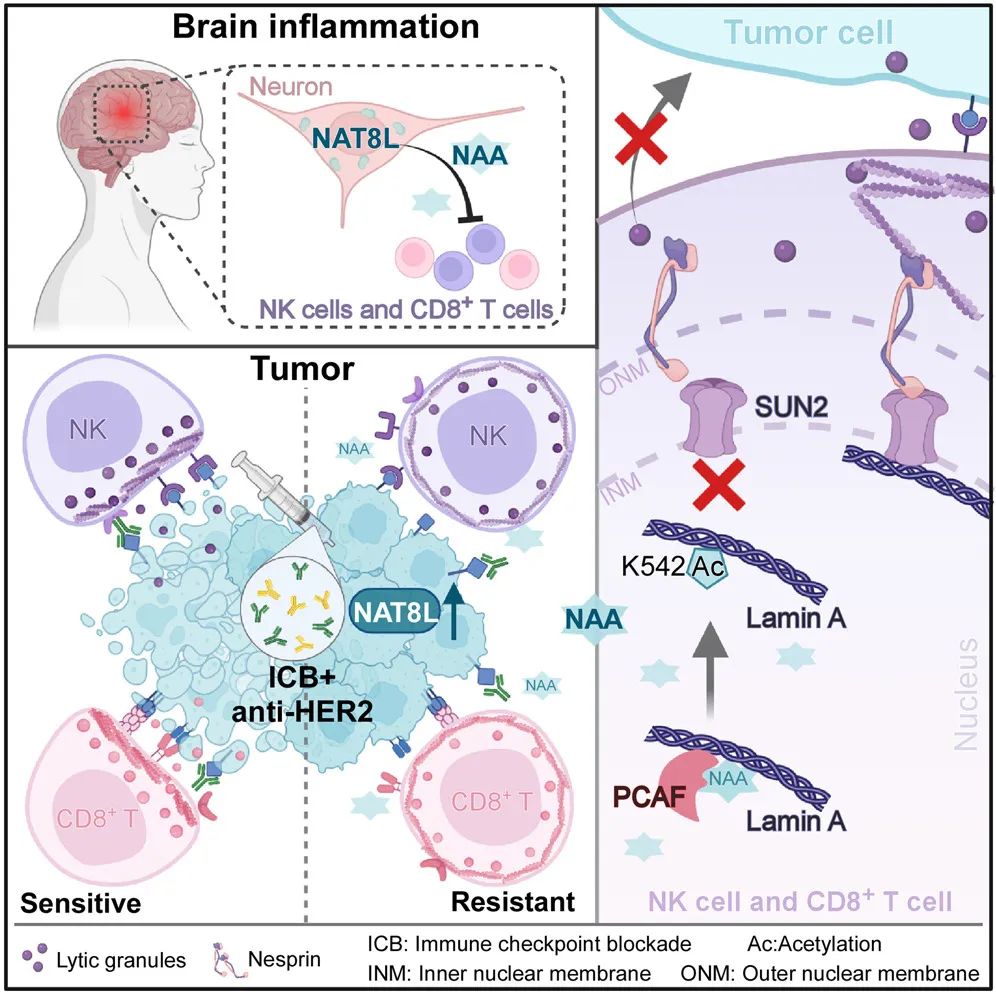
总的来说,这项研究发现肿瘤细胞通过模拟中枢神经系统(CNS)的抗炎机制来逃避抗肿瘤免疫,并揭示了NAT8L是一个潜在的肿瘤免疫治疗新靶点,靶向抑制NAT8L可以增强抗癌药物的疗效。
相关阅读
2023年12月5日,苏士成团队在 Cell 期刊发表了题为:Choroid plexus mast cells drive tumor-associated hydrocephalus 的研究论文【2】。
该研究发现了大脑脉络丛中的一个独特肥大细胞群——脉络丛肥大细胞(CPMC),进一步揭示了这些细胞在致命的脑转移并发症肿瘤相关性脑积水(TAH)中发挥着至关重要的作用,并为TAH提供了一种有吸引力的治疗方法。

2023年12月13日,宋尔卫/苏士成团队在 Nature 期刊发表了题为:Tumour circular RNAs elicit anti-tumour immunity by encoding cryptic peptides 的研究论文【3】。
该研究发现了一种肿瘤细胞特异性环状RNA——circFAM53B,其通过非经典翻译产生的隐性抗原肽,能够有效驱动抗肿瘤免疫,这表明利用肿瘤特异性环状RNA进行疫苗接种,可能是一种针对恶性肿瘤的免疫治疗策略。

2020年9月,苏士成团队等在 Cell 期刊发表了题为:Targeting Mitochondria-Located circRNA SCAR Alleviates NASH via Reducing mROS Output 的研究论文【4】。
这项研究确定了一种线粒体特异性circRNA——SCAR,在非酒精性脂肪性肝炎(NASH)中表达下调,向线粒体特异性递送SCAR,可降低线粒体活性氧(mROS)输出,减轻炎症,可作为NASH的治疗靶标。

论文链接:
1. https://www.cell.com/cancer-cell/abstract/S1535-6108(24)00169-7
2. https://www.cell.com/cell/abstract/S0092-8674(23)01182-0
3. https://www.nature.com/articles/s41586-023-06834-7
4. https://www.cell.com/cell/fulltext/S0092-8674(20)31000-X

